作者简介:刘菲(1969-),女,河北定兴人,教授,主要从事环境监测与地下水污染控制方面的研究. E-mail:feiliu@cugb.edu.cn
面对日益严重的地下水污染,地下水渗透反应格栅技术作为一种原位、简易、被动技术在地下水污染修复中被广泛研究和应用。依据渗透反应格栅技术的定义及发展历程,渗透反应格栅技术的发展大致可以分为2个阶段,即2000年以前的传统零价铁渗透反应格栅阶段和2000年以后的新型复合介质渗透反应格栅阶段。伴随地下水污染形势的日益复杂化,以及渗透反应格栅技术的不断应用和材料科学等其他学科的飞速发展,未来渗透反应格栅技术的发展将主要集中于复合介质与新介质的开发、组合式渗透反应格栅技术的研发、渗透反应格栅技术与其他修复技术的联用以及渗透反应格栅工程的长期监测及管理。
As an in situ, simple and passive technology, Permeable Reactive Barrier (PRB) is becoming widely used in groundwater remediation. Based on its definition and development process, the development of PRB can be divided into two stages: The traditional zero-valent iron PRB before 2000 and the PRB composed of novel mixed media after 2000. With the rapid worsening of groundwater pollution, the increasing application of PRB and the rapid development of materials science, the development of PRB technology in future will be mainly focused on the investigation of mixed and novel media, the design of mixed PRBs, the combination of PRB technology with other remediation technology, and the longterm monitoring and management of PRB projects.
地下水是我国重要的饮用水源[1, 2], 但在我国地下水却面临着严峻的污染形势[3~5]。面对日渐严峻的地下水污染, 针对地下水污染的控制措施和修复技术被广泛研究和应用, 主要包括自然衰减技术、异位修复技术(如抽出— 处理技术)和原位修复技术。作为近年来研究和应用最为广泛的地下水污染修复技术, 原位修复技术是在受污染场地含水层中, 利用各种物理、化学和生物技术就地将污染物去除。据EPA[6]的报告称, 原位修复技术在美国实际污染场地中的应用由1986年的0%增加到1999年的35%。目前, 最主要的地下水原位修复技术包括水力隔离系统、曝气技术、生物降解技术、渗透反应格栅技术、电化学修复技术、原位化学氧化技术、原位热修复技术和植物修复技术等。
作为一种重要的污染地下水原位修复技术, 渗透反应格栅技术(Permeable Reactive Barrier, PRB), 在地下水污染控制与修复中被广泛研究和应用。EPA[7]对PRB给出的定义:是一种埋藏于地下的关于反应材料介质的处理设施, 它被设计用来拦截地下水污染羽, 并为污染羽通过反应介质提供通道, 在这一过程中污染物被转化成环境可以接受的形式, 以实现PRB下游浓度修复的目标。2005年, Interstate Technology & Regulatory Council[8]对PRB也给出定义:广义上, PRB是一种连续的原位渗透处理区并被设计用来拦截和处理污染羽。这种处理区可以直接利用反应介质铁设立(如零价铁, ZVI), 也可以间接通过加入用来激发二级处理过程的介质设立(如通过加入碳源和营养盐来刺激活化微生物的活性), 污染物在PRB中通过物理、化学和生物过程去除。
根据修复机理的不同, PRB可以分为物理、化学和生物PRB, 并进一步分为吸附、沉淀、氧化— 还原和生物降解PRB等。另外, 按结构类型不同, PRB可以分为隔水漏斗— 导水门式PRB和连续式PRB, 其中连续式PRB又可以分为连续墙式PRB和灌注处理带式PRB[6~8]。
在修复污染地下水时, PRB技术具有一定优势:①原位修复技术, 不需额外地面设施; ②简易技术, 在运行过程只需进行定期监测; ③被动修复技术, 只会在设计区域内针对固定污染物产生效果。但是, PRB技术也存在一些不足:①应用深度限制, 一般传统的PRB构建深度不超过30 m; ②PRB去除效果严重依赖于场地地下水流速与反应介质对污染物去除的半衰期, 地下水流速太快或者去除半衰期太长都会造成PRB构建厚度增加。
随着人们环境质量要求的提高, 地下水污染的研究日益成为焦点。根据google文献(http://scholar.google.com.hk)的检索结果(图1), 关于PRB特别是ZVI PRB的研究文献从20世纪90年代左右开始被报道, 并在2000年前后开始被大量研究和关注。据此, PRB的发展历程大致可以分为2个阶段, 即2000年以前的传统ZVI PRB阶段和2000年以后的新型复合介质PRB阶段。
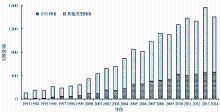 | 图1 1993— 2014年PRB研究文献统计(数据来自Google文献http://scholar.google.com.hk)Fig.1 Statistics of PRB reference from 1992-2014 (Data collected from Googlehttp://scholar.google.com.hk) |
(1)传统ZVI PRB阶段(2000年以前)
氯代烃(四氯化碳)与金属(锌)的反应, 早在20世纪40年代就被研究和报道[9, 10]。1972年, Sweeny 等[11]报道称粒状锌可以与DDT、林丹和氯丹等有机氯农药发生脱氯反应。随后, 氯代烃的脱氯产物在锌与四氯化碳的反应中被检测到[9, 10]。1990年, 加拿大滑铁卢大学Reynolds等[12]在研究井管以及其他取样设备对采集受氯代烃污染地下水样品的影响时发现, 在使用不同金属材料设备取样时也存在氯代烃与金属取样设备之间的脱氯反应。据此, 加拿大滑铁卢大学Gillham等[13]在1992年提出可以利用ZVI来修复受氯代烃污染的地下水, 并通过后续实验证明一些过渡金属(如ZVI)可以与除二氯甲烷以外的13种卤代烃发生脱卤反应。1991— 1996年, 第一个由ZVI还原三氯乙烯(TCE)和四氯乙烯(PCE)的野外中试试验研究在加拿大安大略省Borden空军基地进行[14]。
1995年1月, 第一个商业化修复地下水中氯乙烯、二氯乙烯和TCE的ZVI PRB在美国加利福尼亚州Sunnyvale成功实施, PRB特别是ZVI PRB开始广泛受到关注[15]。截止2005年, 全世界范围内关于ZVI PRB的工程已有120个, 其中有83个为商业化修复工程[8]。到2010年, 全世界范围内的ZVI PRB的工程达到200多个, 其中商业化修复工程达150多个[16]。
(2)新型复合介质PRB阶段(2000年以后)
随着ZVI PRB技术的广泛应用和发展, ZVI PRB技术逐渐被认可并成为一种标准地下水污染修复技术。但由于污染地下水中污染物成分复杂, 许多污染物并不能通过ZVI PRB去除(如苯系物[17])。同时, ZVI PRB在某些特殊污染场地对污染物的去除效率受水文地质条件的严重制约和影响。
因此, 一些新型复合介质PRB在2000年前后开始被重点研究和开发, 这些活性介质大致可以分为铁基型和非铁型反应介质2类:①铁基型反应介质, 主要有铁的双金属(铁— 镍双金属系统[16, 18~20]和纳米铁等[16, 18, 20, 21]; ②非铁型反应介质, 主要有活性炭、沸石、石灰石、磷灰石以及与微生物相关的营养盐和碳源等[18, 20]。此时, PRB技术不仅简单局限于ZVI PRB, 还包括吸附PRB、生物降解PRB等, 也被用来治理各种地下水中的污染物(如苯系物[17, 22]或只是被设计用来改变污染场地内的地下水化学条件(如调整地下水pH, 转换地下水氧化还原条件等[18]。
传统铁基型PRB技术主要以ZVI作为PRB反应介质, 通过ZVI与污染物之间的还原反应实现污染物的去除。根据Ritter等[23]的双层模型理论, ZVI表面通常存在一层约2.25 μ m厚且成分不稳定的氧化层/钝化层, 由内外2层构成, 内层为磁铁矿(Fe3O4), 外层为更高价态铁氧化物(赤铁矿/Fe2O3和磁赤铁矿/γ -Fe2O3)。当ZVI与水接触后, 外层的钝化膜首先被自动还原, 形成Fe2+和/或转化为磁铁矿(公式1)。磁铁矿是导体, 可以允许电子通过。但是, 赤铁矿和磁赤铁矿一般被认为是半导体或者绝缘体, 不允许电子通过。
Fe→ Fe2++2e-阳极反应
12Fe2O3+ 8H++8e- → 8Fe3O4 + 4H2O 阴极反应
Fe2O3 + Fe+ 6H+ → 3Fe2+ +3H2O (1)
传统铁基型PRB中, 主要是通过ZVI的还原以及PRB内的沉淀、吸附、络合以及共沉淀等作用实现污染物的去除[18], 但Noubactep[24]认为ZVI PRB主要的去除机理是共沉淀而非脱氯还原。目前, ZVI PRB已经被用来处理地下水中的氯代烃类、重金属类、放射类、营养盐类、硝基芳香烃类污染物以及偶氮和蒽醌类染料。关于ZVI PRB去除氯代烃的研究, 国内外都有了丰富实验研究和工程应用资料, 效果非常明显[6~8, 25, 26]。
与ZVI相关的单纯脱氯还原反应是在ZVI表面发生的阴阳两极反应的总和, 如果脱氯反应完全, 就会生成烃类(公式2); 同时, ZVI与水也会发生类似的阴阳两极反应, 并生成H2和OH- [16](公式3)。在ZVI与氯代烃的还原脱氯过程中, 系统氧化还原电位(Eh)会从初始约-400 mV迅速降低至约-500 mV[23], 并使pH增加至> 9.0[27]。Wilkin等[26]在监测运行15年的ZVI PRB时发现, PRB内和下游地下水pH至少分别增加2个和1个单位, Eh则至少分别减少50 mV和200 mV。
Fe0 → Fe2++2e- 阳极反应
RCl+2e-+H+ → RH+Cl- 阴极反应
Fe0+RCl+H+ → Fe2++RH+Cl- (2)
Fe0 → Fe2++2e- 阳极反应
2H2O+2e-→ H2+2OH- 阴极反应
Fe0+ H2O → Fe2++ H2+2OH- (3)
以ZVI对PCE的还原脱氯为例, PCE可以通过α -消去和β -消去2种途径实现逐级脱氯, 并伴随有氢解反应和加氢反应[16]。但在实际工程中, ZVI对PCE的还原脱氯主要以β -消去为主[27], 生成的中间产物有TCE, 二氯乙烯、氯乙烯, 并最终被还原为乙烯和乙烷[16, 28]。同时, Gilham等[16]认为氯乙烯是控制ZVI PRB设计的主要因素。
ZVI与氯代烃的脱氯反应是发生在ZVI表面的界面反应, 故其脱氯速率首先受ZVI比表面积的影响。而且, 脱氯反应会消耗H+并生成H2和OH-, 所以pH也会影响脱氯速率。同时, PRB内的沉淀与气体可能会影响ZVI比表面积, 进而影响脱氯速率。另外, 所有界面反应中必须包括传质过程[29], 故温度、阴阳离子、表面活性剂、腐殖酸和共存有机物也会影响脱氯速率。
ZVI类型及其比表面积:Gilham等[16]指出ZVI与氯代烃的脱氯反应必须有Fe0存在。同时, ZVI脱氯速率随比表面积的增加而加快[30~32]。通过酸洗、H2还原和超声波等表面预处理手段, 可以将ZVI表面氧化层剥离并提高脱氯速率[33~36]。另外, 脱氯过程中会有气体和沉淀生成并影响ZVI比表面积, 有时气体比沉淀所造成的比表面积损失要大[37]。但是, Vikesland等[38]研究认为沉淀和气体对ZVI PRB寿命的影响远小于ZVI自身的钝化。
pH:ZVI与氯代烃的脱氯需消耗H+, 所以地下水中较低pH可提高脱氯速率[7]。但是, 研究不同pH下ZVI对四氯化碳的还原发现, 即使pH升高1个单位, 脱氯速率的降低也不十分明显[31]。高pH虽使四氯化碳的脱氯速率降低, 但也使有毒的不完全脱氯产物的积累减少[36]。而且, 降低pH虽然使ZVI还原硝基苯的速率加快, 却不能将之还原为苯胺[30]。Chen等[39]研究亦指出, 较低pH固然能提高TCE还原脱氯速率, 但伴随着ZVI酸蚀加剧, 比起较高pH并无优势。另外, pH并不是比表面积降低的主要因素[40], ZVI比表面积的减少并没随pH的升高而线性减小[36]。
温度和溶解氧(DO):ZVI对氯代烃的脱氯符合Arrhenius方程, 当温度由25 ℃降低至10 ℃时, TCE的脱氯速率降低约4倍[16]。DO可以将Fe2+氧化成Fe3+, 并抑制ZVI的还原效率。但事实上, TCE的氧化性能与O2相似[9], DO对ZVI脱氯速率的影响并不大[41, 42]。
地下水主要成分:相比于去离子水, 地下水中ZVI对TCE具有相对较高的脱氯速率[43]。① NO3-。NO3-由于具有更高的氧化性而会优先和ZVI反应, 并与TCE竞争ZVI表面反应活性位点, 进而抑制ZVI对氯代烃的脱氯[8, 23, 44]。但是, 当有低压电流(< 36 V)导入时, ZVI不易被NO3-钝化[45]。②CO32-和HCO3-。Gilham等[16]认为在实际脱氯过程中, HCO3-可以增加体系对pH的缓冲, 并可促进ZVI的腐蚀而提高脱氯效率[46]。但是, 刘玉龙[47]认为HCO3-和CO32-在促进ZVI腐蚀的同时, 会生成沉淀并吸附在ZVI表面进而降低脱氯速率, 二者同时存在, 此消彼长, 后者很快占据优势并降低脱氯速率。③Ca和Mg。地下水中Ca和Mg会形成沉淀并沉积于ZVI表面。特别是有腐殖酸共存时, Ca和Mg会明显促进金属氢氧化物和腐殖酸的团聚, 使之沉积于ZVI表面并改变PRB渗透性, 降低ZVI脱氯速率[47]。但是, Weber等[46]却认为菱铁矿和文石等矿物沉淀会严重阻滞ZVI的腐蚀, 相比于生成的文石晶体, Ca可以与菱铁矿等矿物沉淀竞争CO32-, 更有利于ZVI的长期腐蚀。④ Cl-, SO42-和其他离子。在氯代烃脱氯反应中, 会有Cl-生成并可能抑制反应的进行。Reardon[48]研究发现HCO3-, SO42-或Cl-对ZVI脱氯速率的影响顺序为HCO3-> SO42-> Cl-。但是, Farrell等[27]却发现SO42-和Cl-对TCE脱氯速率的影响在95%置信度范围内没有统计学上的差异。同时, 也有研究发现加入NaCl[49]或Na2SO4[50]可显著提高四氯化碳的脱氯速率。地下水中PO43-, BO33-和H2SiO4会提高ZVI的腐蚀速率(PO43- > BO33-> H2SiO4[51]), 但是Kohn 等[52]却发现0.5 mM的硅可使ZVI对TCE的脱氯效率降低65%, 并改变TCE脱氯产物比例和ZVI表面腐蚀矿物种类。
腐殖酸和表面活性剂:腐殖酸可使ZVI脱氯速率降低, 且有Ca2+, Mg2+存在时, 腐殖酸和金属氢氧化物的团聚明显并在ZVI表面沉淀而影响脱氯速率。阳离子表面活性剂浓度在临界胶束浓度以下, 可增强氯代烃的脱氯速率, 但过高浓度的表面活性剂会占据ZVI表面的反应活性点而降低脱氯速率; 经表面活性剂预处理的ZVI, 其还原脱氯速率比直接将表面活性剂与ZVI在水中简单混合的要高。阴离子和非离子型表面活性剂降低ZVI的还原速率[47]。同时, 表面活性剂的存在使ZVI对PCE的脱氯还原过通过β -消去转变为氢解反应, 并导致较高中间产物TCE的积累[53]。
共存有机污染物:在污染地下水中, 几种物化性质完全不同的污染物可能会同时存在于同一污染羽, 并可能影响ZVI脱氯速率。Dries等[54]研究发现苯和甲苯可使PCE的脱氯速率提高50%, 并对TCE的脱氯略有促进作用。但是, 刘玉龙[47]却发现苯的存在会使PCE以及PCE和TCE混合的脱氯速率提高, 并使TCE的脱氯速率降低; 甲苯则始终抑制PCE和TCE的还原脱氯。Clark等[55]发现乙醇可提高PCE在水中的分配系数, 降低铁表面吸附PCE浓度, 从而降低对PCE的还原速率。
微生物:对于ZVI PRB中微生物的作用, 不同的研究者有不同的结论[56]:①促进作用。PRB内反硝化细菌会利用NO3-并减弱其对ZVI的钝化以及与氯代烃的竞争。而铁还原细菌会将Fe3+还原生成Fe2+, 并可能生成对氯代烃去除活性更高的绿铁锈。硫酸盐还原菌的存在会产生铁的硫化物, 这有利于提高PRB活性[57]。同时, Dehalococcoides sp.和Desulfuromonas sp.等菌种还可以通过共代谢等生物降解途径去除地下水中的氯代烃[58]。另外, 大量生物质的存在还可能会增加PRB内污染物的吸附, 促进PRB内污染物的去除。而且, 在微生物新陈代谢过程中会产生大量的酸性物质, 这有利于降低ZVI PRB内pH, 进而促进ZVI表面氧化膜和沉淀的溶解, 提高脱氯效率。②抑制作用。微生物会在PRB内富集生长并产生大量生物质, 且微生物新陈代谢活动还可以在PRB内生成大量气体(N2和H2等)和沉淀(FeS和CaCO3等), 进而降低PRB水力性能[59, 60]。同时, 微生物本身及其产生的沉淀和气体还可以吸附在ZVI表面, 与污染物竞争ZVI表面的反应活性位点进而阻断ZVI和污染物之间的电子传递, 间接造成ZVI钝化[61]。另外, 微生物还可能会直接从ZVI表面吸收电子氧化ZVI, 加快ZVI钝化过程[25, 62]。
ZVI的Eh一般为-200~-500 mV[16], 它不仅可以用来还原去除氯代烃, 还可以用来还原去除地下水中的一些重金属类及放射类污染物[18, 62], 如铬(Cr)、砷、镉、铅、铜和铀等。目前, ZVI PRB已经被成功用于现场修复Cr6+污染的地下水, 原理如公式4所示[62]:
CrO42-+Fe0+8H+ → Fe3++Cr3++4H2O
(1-x)Fe3++(x)Cr3++2H2O → Fe(1-x)Cr(x)OOH↓ +3H+ (4)
在ZVI还原去除Cr6+的过程中, 系统Eh会迅速从初始的> 100 mV降低至< -300 mV。在美国Elizabeth City市ZVI PRB修复Cr6+和TCE污染地下水的工程中, Cr6+在TCE先被脱氯还原后才开始被还原沉淀, ZVI使地下水Eh降低至-600 mV, pH由5.8~6.5升高至9.5~11[62]。在利用ZVI PRB去除地下水中的镍时, Bilardi等[63]认为a-FeOOH是造成去除速率下降的主要因素。在去除其他重金属类及放射类污染物时, ZVI也都是先通过还原反应将重金属类及放射类污染物还原转变为低价态, 并进一步被直接或络合沉淀去除[32, 63~70]。同时, 这一过程中还存在吸附、表面络合以及共沉淀等作用[18]。
在处理一些营养盐类污染物时(NO3-和SO42-), ZVI还可以将NO3-还原为NH4+(公式5)[71~74]。当ZVI PRB中有硫酸盐还原菌存在时, 55%的SO42-可以在PRB中被去除[75]。同时, 在实际ZVI PRB工程中, 均发现由硫酸盐还原菌造成的SO42-的减少[25, 26, 76, 77]。
NO3-+3Fe0+H2O+ 2H+ → NH4++Fe3O4
NO3-+12Fe2++13H2O → NH4++4Fe3O4 + 22H+
NO3-+2.8Fe0+0.2Fe2++2.2H2O → NH4++1.2Fe3O4 + 0.4OH- (5)
利用ZVI PRB, 还可以处理硝基芳香烃类污染物, 如硝基苯, 二硝基甲苯和三硝基甲苯等, 并最终将硝基芳香烃类污染物还原为芳香胺类化合物[78~80]。与ZVI PRB还原NO3-相似, ZVI只是将硝基芳香烃类污染物中的还原成-NH2或-NH。另外, Fu等[79]报道称, ZVI还可以去除一些偶氮和蒽醌类染料。Epolito等[81]在研究ZVI对蒽醌染料Reactive Blue 4的脱氯反应发现, 脱氯速率的增加与体系pH的降低、温度的升高以及离子强度的增加有关, 并认为离子强度对ZVI脱氯速率的迥异影响与污染物类型有关。
随着PRB技术的迅速发展, 用于PRB的反应材料不仅局限于ZVI, 还包括纳米铁(NZVI)、生物降解PRB材料(如碳源、释氧材料和营养盐等)、活性炭、沸石、石灰石等碱性材料、磷灰石、连二亚硫酸钠(NaS2O4)以及改性红泥等。Obiri-Nyarko等[18]总结认为, 活性炭可以用来吸附处理苯酚、苯系物、氯代烃以及重金属等多种污染物, 但其主要机理是吸附, 受pH和有机质等因素的影响。沸石通过阳离子交换作用可以去除地下水中的钠、钾、Ca、Mg、铅、铜和镉, 经过改性的沸石则可以被用来去除地下水中的重金属、NH4+、NO3-、PO43-、PCE、铀及苯系物等。通过石灰石等碱性材料, 可以增加地下水pH, 使酸性采矿废水中的某些离子转化为沉淀而去除。磷灰石含有大量的磷和钙的化合物, 可通过静电吸附或离子交换去除某些阳离子污染物, 也可以通过沉淀或者吸附来去除其他污染物, 如铅、砷和铀。与ZVI相似, NaS2O4具有一定的还原性, 可还原Cr、铀等污染物。将红泥通过卤水改性, 就可制得改性红泥, 改性红泥可以用来取代石灰石进行酸性采矿废水的处理。
腐殖质材料:腐殖质材料(如活性炭、泥炭、锯末、褐煤亚烟煤和生物质炭等)和一些金属氧化物(如磁铁矿、赤铁矿等)由于具有较高的比表面积和良好的吸附性能, 可以在PRB中作为吸附剂去除污染物[82]。Arora等[83]利用活性炭去除严寒地区地下水中甲苯时发现在4 ° C时活性炭对甲苯的吸附速率比20 ° C时显著降低(3.65 × 10-13 m2/s VS 5.112 × 10-13 m2/s)。在活性炭中注入20%硫酸或者由二氧化硫处理过的活性炭可以显著提高PRB对地下水中汞的处理效率[84]。在实际PRB工程中, Bortone等[85]在灌注处理带式PRB中加入活性炭作为反应介质, 用来处理受四氯化碳污染的地下水, 结合实验数据模拟发现在70年时间内PRB下游PCE的浓度可以始终达标。
沸石:沸石由于具有较高的吸附能力以及廉价性, 经常被用于PRB中。Vignola等[86, 87]利用沸石PRB去除受石油烃(苯系物、多环芳烃和甲基叔丁基醚)污染的地下水, 处理后的污染物浓度均可以达标。同时, 沸石PRB可以有效去除地下水中的NH4+, 并被成功应用于实际地下水修复工程[88, 89]。但是, 由于天然沸石吸附污染物的机理主要为阳离子交换, 因此, 天然沸石只对地下水中的阳离子类污染物有很强的去除能力。通过表面改性后的沸石, 相比于天然沸石不仅具有很强的阳离子吸附能力, 而且可以高效吸附去除地下水中的阴离子、非极性类有机污染物以及细菌等。另外, 沸石PRB去除机理单一, 吸附饱和后便失去对污染物的去除能力, 需通过反冲洗等其他手段对沸石进行活化。因此, 沸石常被作为PRB的部分反应介质, 以在PRB运行初期实现对污染物的快速去除。在生物降解PRB中, 微生物在沸石表面的挂膜会严重影响PRB的效率, 可以将微生物生长的所需的碳源和电子供体/受体提前负载至沸石表面[90]。
微生物碳源及电子受体/供体:通过微生物的新陈代谢活动[91], 可以将一些污染物作为微生物的碳源(如苯系物)或者电子供体(如O2、NO3-、SO42-)而被去除, 或通过微生物的新陈代谢活动改变地下水的地球化学条件(如升高pH、生成S2-), 进而使某些污染物去除(如银、镉、铜、铅、铁和镍等)。通过生物降解PRB, 还可以修复一些酸性采矿废水[92]。Benner等[93]利用装填有砾石、木屑及树叶的PRB去除受Fe2+、SO42+、镍以及pH(5~6)污染的地下水, 最终SO42+被硫酸盐还原菌还原并与生成铁的硫化物沉淀而去除。Robertson等[94]在监测运行15的处理NO3-的PRB后, 发现15年内NO3-的去除速率在不同温度下为0.22~1.1 mg N/L/d(6~10 ℃)和3.5~6.0 mg N/L/d(20~22 ℃), 在运行15年后 NO3-的去除速率由于受到碳源(木屑)的影响而降低80%。Lojkasek等[95]和Xin等[96]分别构建了生物降解PRB, 用以修复地下水中的TCE和苯系物。在利用生物降解PRB修复地下水时, 去除效率主要受到微生物碳源、电子供体以及地下水环境(pH、温度和盐度)的影响。作为微生物最容易利用的电子受体O2, 在地下水修复时通常通过井内曝气、加入释氧材料(ORC)等方式来提高地下水中的DO, 以促进PRB中的生物降解效率[18, 97~100]。ORC作为一种简便、高效的增加地下水中DO的技术, 已经被广泛研究并实际应用于地下水修复中[88, 89, 101]。
随着PRB技术的不断发展, 为进一步提高PRB处理效率或降低PRB建造成本, 各种新的反应介质开始被应用在PRB中, 如铁的双金属材料、纳米铁材料、复合材料等。一些在自然界分布广泛的矿物材料, 由于具有一定的去除效率且价格低廉, 也开始被尝试应用于PRB[82, 102]。
ZVI的双金属材料:最早发现具有脱氯作用的金属并不只有ZVI, 加拿大滑铁卢大学Reynolds等[12]和Gillham等[13]就报道称一些过渡金属均可与氯代烃发生脱氯反应。随后研究发现锌、镍、铅、铜和钴等金属均对ZVI的脱氯反应有催化作用, 这些金属常被用来与ZVI形成双金属系统, 或者被通过化学沉淀、电镀等方法沉积到ZVI表面形成双金属系统, 以提高ZVI脱氯速率[47]。与单纯ZVI材料相比, 虽然双金属材料在地下水污染修复时具有较高的效率, 但由于受到PRB成本的限制, 在实际PRB工程中双金属材料并未被应用。
纳米铁(NZVI)或微米铁(MZVI)材料:NZVI(nm)或MZVI(μ m)材料由于具有更高的比表面积和反应速率而被用于地下水污染修复中。NZVI可以用于修复氯代烃、苯和乙烷等污染物形成的污染羽[8, 103~105], 也可以用于DNAPL类污染源的修复[104], 还可以用于去除水中的偶氮和蒽醌类染料[106, 107]。1997年, Wang等[21]首次将NZVI应用于去除地下水中的PCE和TCE。Gilham等[16]认为将NZVI注入地下含水层后, 其反应活性并不能持续数月或者数周, 且NZVI成本昂贵, 不易重复注射。Johnson等[108]研究发现, 在稳定地下水流速下NZVI在含水层中最远可以迁移2.5 m, 但是大部分NZVI在1 m的范围内就被完全氧化失效, 仅2%的未被氧化的NZVI可以迁移至2.5 m处。因此, NZVI作为修复材料目前一般用于污染源的修复, 或者一些需要在短期内高效去除大量污染物的污染场地。将NZVI负载于多孔介质形成复合介质, 并可以作为反应介质构成NZVI PRB[109]。目前, 一些新的NZVI预处理技术也开始被研究和开发, 以提高NZVI对污染物的去除速率。在H2环境中, 将NZVI在550 ℃下加热3 h, 可以有效去除NZVI表面的针铁矿, 并提高NZVI对Cr6+的去除速率[110]。将NZVI与黄原胶混合, 可以有效防止NZVI在应用初期被氧化[111], 压力3.5 bar时含油30 g/L NZVI的黄原胶溶液在石英砂含水层中可以迁移约7 m[112]。但是, 随着NZVI的不断研究和应用, NZVI的生物毒性也逐渐被研究和关注[113~115]。针对NZVI在地下水修复中的一些缺陷, MZVI开始被研究并应用于污染地下水修复, 而且一些聚合物(如瓜尔胶)也被应用于MZVI以缓解其在应用初期的沉淀和氧化[116, 117]。Comba等[118, 119]研究发现, 有瓜尔胶存在时MZVI在石英砂含水层中最远可以迁移2 m。与NZVI相比, MZVI更容易在含水层中迁移[120]。但是, 通过研究对比MZVI与NZVI的产氢速率发现, NZVI的氢气产生量要比MZVI高出2倍, 当有Pb等双金属材料存在时, NZVI的氢气产生量要比MZVI高出2~39倍[121]。
双金属纳米材料:NZVI和其他金属(镍、铜、银和锌等)构成的双金属纳米材料也被直接或者负载在具有较大比表面积的多孔介质中, 以去除地下水中的氯代烃和重金属类污染物[122~125]。Xu等[126]研究发现, 通过球磨制成的镍— 铁双金属纳米材料可以有效去除地下水中的4-氯苯酚, 且去除速率高于化学合成法制成的镍— 铁双金属纳米材料, 同时脱氯速率随着双金属系统中镍比例的增加而提高。另外, 当pH> 7时就可以显著观测到镍— 铁双金属纳米材料的钝化。
亚铁类矿物:亚铁类矿物(如FeS)可以被用来去除地下水中的一些金属类污染物和氯代烃类污染物[127~132]。Henderson等[133]的研究发现, 在利用FeS作为PRB介质时, 由于沉淀和气体导致的PRB渗透性能的损失分别为1%和30%。
混合反应介质:在利用PRB处理地下水中污染物时, 有时某种反应介质对某种污染物的去除效率有限, 需要结合其他材料来提高对污染物的去除速率; 或者地下水中经常会出现几种物化性质不同的污染物共存的情况, 仅通过某一种反应介质很难实现对污染物的去除。因此, 随着PRB技术的发展, 各种混合介质也被开发和应用。Ludwig等[70]将ZVI、砾石、树叶与石灰石混合, 构建PRB以去除地下水中的砷、重金属和酸度。在修复华盛顿州Hanford Cr6+污染场地时, Oostrom等[134]将MZVI与聚合物混合形成混合溶液以增加MZVI在PRB中的流动性, 并在其中加入一些多孔介质材料来提高PRB的渗透性。Yang等[135]利用二甲基二氯硅烷改性后的活性炭, 结合ZVI构成PRB, 用来处理地下水中的2, 4-二氯苯酚, 并最终将2, 4-二氯苯酚在PRB中被还原为2-氯苯酚、4-氯苯酚或苯酚。将活性炭、沸石和ZVI混合, 组成复合PRB反应介质(最佳比例4:1:5), 可以去除垃圾渗滤液中55.8%的COD、70.8%总氮(TN)、89.2%的NH4+、70.7%的镍、92.7%的铅和94.2%的16种多环芳烃[136]。
在利用PRB修复地下水中的污染羽时, 有时会有几种物化性质截然相反的污染物同时存在于污染羽中, 此时很难通过单一机理将污染羽修复。Chen等[5, 17]将ZVI PRB与生物降解PRB联合, 可以有效处理受氯代烃(TCE)和苯系物形成的地下水混合污染羽。
另外, 在利用好氧生物降解PRB修复地下水时, 由于地下水DO相对较低, 则需要通过释氧材料(ORC)来为微生物供氧。但是, 由过氧化钙或过氧化镁等过氧化物制成的PRB通常会造成地下水中pH的升高并影响微生物活性。所以在实际应用ORC材料和好氧生物降解PRB时, 常将ORC材料与微生物PRB顺序前后设置, 构成释氧— 好氧生物降解组合式PRB, 以修复污染地下水[88, 89, 137]。另外, 也可以在好样生物降解PRB前设置曝气井, 增加地下水DO[138]。
PRB与自然衰减技术联用处理地下水污染羽:在利用PRB修复地下水污染羽时, PRB内的反应介质可以迅速将高浓度污染物降解并遵循去除动力学方程。但是, 对于剩余浓度较低的污染物, 要实现在PRB内的完全去除(至未检出), 按照去除动力学方程则需要相当长的时间并因此导致PRB处理周期和建设成本的增加。将PRB与自然衰减技术联用, 通过PRB先将地下水中的高浓度污染物迅速降低至较低浓度, 然后通过监测PRB下游污染物的自然衰减, 可以在很大程度上优化PRB设计并节约PRB成本[16]。
PRB与帷幕技术联用处理污染源区:在处理地下水中污染源时, 某一些污染源很难被挖掘和转移处理, 这时通过帷幕技术先将污染源控制以防止污染物继续向四周扩散, 同时在污染源某一侧设计建造PRB, 在污染源污染物渗透穿过PRB时实现污染物的去除。在用ZVI PRB与帷幕技术联合处理污染源时, 也可以将粘土、ZVI与污染源直接混合, 首先通过粘土来减少污染物向四周的迁移扩散, 然后再利用ZVI去除溶解态的污染物[16]。
与水力控制技术联用:PRB是一种被动修复技术, 在利用PRB修复地下水污染羽时, 污染地下水只有穿过装有反应介质的PRB, 污染物才可以被去除。因此, 在设计PRB时常由于污染羽覆盖范围很大而很难使所有污染羽都穿过PRB。通过与水力控制技术联合, 可以人为控制和干预污染地下水的水力特性, 使更多污染地下水穿过PRB[16]。
与化学氧化技术的联用:将PRB技术与化学氧化技术联用, 先通过PRB中的吸附材料将地下水中的污染物吸附, 然后通过化学氧化技术向PRB中注入强氧化剂, 氧化被PRB吸附的污染物并活化吸附剂[139~142]。Do等[143]利用一种由废弃物制成的吸附剂先吸附地下水中的苯系物, 然后向PRB中注入有H2O2/Fe3+/草酸盐的氧化剂, 可以有效氧化被吸附的苯系物并实现吸附剂的活化。
与物理技术的联用:将物理技术技术(磁化技术、超声波技术等)与ZVI结合, 可有效提高ZVI对一些金属类污染物的去除速率。将超声波技术与ZVI PRB联用, 可有效提高偶氮和蒽醌类染料的去除速率[79]。Jiang等[144]在利用ZVI去除溶液中的Cu2+时, 通过加入一定的弱磁场可将ZVI对Cu2+的去除速率提高10.8~383.7倍, 磁场有利于ZVI的腐蚀和Eh的降低。同时, ZVI与磁化技术联用也被用来去除溶液中的铯[145, 146], 并发现在pH=6条件下经2-(N-morpholino)ethanesulfonic acid(MES)老化处理6~60 h的ZVI, 在有弱磁场存在时可将ZVI对铯的去除速率提高10~100倍。
与电修复技术联用处理地下水污染羽或污染源:电修复系统按电极两端所加载电势强弱可以分为3类:①电— 热修复技术, 是两电极之间通过加载高电压(> 110 V)而对固定区域加热, 使污染物挥发去除; ②电动力学修复技术, 是在两电极之间加载36— 110 V电压, 以刺激或者促进不同带电性的污染物分别向2个电极运动, 然后通过电极附近的氧化还原反应等去除污染物; ③电解还原修复技术, 是在2个电极之间加载低压直流电流(< 36 V), 以在固定区域内形成弱电场并促进区域内电子的迁移转换, 此时两极之间的土壤颗粒等介质本质上只是作为弱电场内的电容存在[54]。Ruiz等[147]将电动力学修复技术和活性炭PRB联合处理粘土中的2, 4, 6-三氯苯酚, 粘土中的2, 4, 6-三氯苯酚在电流的推动下向活性炭PRB迁移, 并在活性炭PRB中被吸附去除。将电动力学修复技术与含沸石PRB结合, 可以有效去除地下水中的NO3- [148]。同时, Mena等[149]将电动力学修复技术和生物降解技术结合, 用来修复受柴油污染地下水。将电解还原修复技术与ZVI PRB技术联合, 在阴极附近可以提高脱氯速率, 同时阴极还可能有利于ZVI PRB中已钝化ZVI的还原[150]。
作为一种地下水污染原位修复技术, PRB的运行寿命是关乎PRB实际工程应用的另一个重要问题。随着PRB特别是ZVI PRB在地下水污染修复工程中的广泛应用, 关于PRB长期运行监测及管理的研究开始受到关注。通过监测丹麦Funen Island运行7年的ZVI PRB发现[58], 7年后PRB对主要氯代烃(PCE、TCE和1, 1, 1-三氯乙烷)的去除率仍> 99%, 但脱氯中间产物cis-二氯乙烯的累积导致PRB对cis-二氯乙烯的去除率偏低。同时, 在PRB内发现有铁还原菌和硫酸盐还原菌的存在并认为可能存在有微生物脱氯过程。另外, PRB内ZVI腐蚀产生的沉淀以及微生物是限制PRB长期运行的重要因素。Phillips等[25]监测在北爱尔兰Nortel Network site连续运行10年(1995— 2006年)的去除TCE的ZVI PRB发现, 运行10年后PRB仍能将地下水中的TCE降低至未检出, 但在ZVI表面发现有钙和铁的碳酸盐、铁的硫化物以及铁的氢氧化物沉淀。在对PRB中微生物菌落的分析发现, PRB内部主要的微生物菌种有反硝化细菌、硫酸盐还原菌和铁还原菌等, 且PRB内前部微生物菌落的多样性要好于后部(可能与后部较高pH环境有关)。同时, 他们认为硫酸盐还原菌和铁还原菌有利于ZVI PRB去除效率的提高。另外, 通过计算发现ZVI PRB前半部分(0-25 cm)的运行寿命约在2-5年, 而后半部分至少有> 10年的运行寿命。通过监测美国Elizabeth City市去除地下水中Cr6+和TCE的ZVI PRB发现[26], 运行15年后ZVI PRB仍可去除90%的TCE和> 90%的Cr, 并可以有效去除地下水中的CO32-、SO42-、NO3-、Ca、Mg及硅, TCE主要脱氯副产物有cis-二氯乙烯、氯乙烯、乙烯和乙烷等, 且在运行15年后并没有观测到PRB内水力传导性能的显著减少。
对于其他类型PRB, Vignola等[86]通过监测运行1年的沸石PRB发现, 6个月内沸石可以有效将地下水中5 mg/L的石油烃(主要是苯系物和多环芳烃)、5 mg/L的甲基叔丁基醚以及无机离子(8537 mg/L的Na+和10700 mg/L的Cl-)吸附去除, 通过反冲洗可以有效活化沸石的吸附能力并去除沸石表面的微生物膜。通过监测运行15年的去除NO3-的PRB发现[94], 填充有砂砾和木屑的PRB可以有效去除地下水中的NO3-, PRB内的反硝化速率受到温度的显著影响, 当反应柱内木屑消耗殆尽时反硝化速率的降低达80%。
虽然PRB已经开始在地下水污染修复中广泛应用, 特别是ZVI PRB, 但在PRB技术的研究和应用方面还存在许多不足, 需要通过全面、系统、长期和连续的监测, 来获取各种类型PRB实际运行过程中的相关数据, 以对PRB技术做出科学评价。PRB的监测包括在PRB建设前、运行中以及运行后对场地水文地质参数(如水力传导性能、地下水流速流向等)、地下水水文地球化学条件(如pH、DO、氧化还原电位、无机离子和有机物等)、污染物的迁移转化(污染物沿地下水流向浓度的迁移变化、各种副产物沿地下水流向的迁移积累)以及微生物特征进行监测。同时, 为评价PRB的长期运行效果, 还需要对PRB内反应介质的变化、沉淀的积累、污染物的去除中间产物的累积以及地下水水文地球化学条件的变化进行全面监测, 以了解反应区污染物的去除机制, 并对PRB的运行效果进行全面评价。
自1992年ZVI PRB在实验室开始被用于地下水污染治理以来, PRB已经被广泛应用于地下水污染控制与修复中。目前, 在欧美等发达地区, 商业化PRB特别是ZVI PRB工程已经在实际地下水污染治理中广泛推广。但在我国, 除在沈阳、焦作由中国地质大学(北京)完成2处PRB的示范工程外(其中焦作为中试规模)[88, 89], 尚无任何商业化PRB工程在地下水修复中的应用。商业化PRB修复工程将是未来PRB技术在我国发展的重要方向。针对特殊地区(如地下水埋深较深地区)复杂污染场地(非均质含水层)地下水污染修复PRB技术的工程应用及优化也将是未来国内外研究的焦点[151]。同时, 关于PRB设计、施工及运行过程中的数值模拟也是未来研究的热点, 特别是针对复杂水文地质条件下PRB水力性能及污染物去除的模拟。
另外, 根据国外PRB技术研究和发展, 关于PRB技术中复合介质与新介质的开发, 组合式PRB技术的应用, PRB与其他修复技术的联用, 以及PRB的长期运行监测及管理将仍然是未来PRB技术研究的重点。PRB技术中不同类型污染物在PRB的修复机理与长期运行效果的评价, 也需要进一步深入研究。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|
| [61] |
|
| [62] |
|
| [63] |
|
| [64] |
|
| [65] |
|
| [66] |
|
| [67] |
|
| [68] |
|
| [69] |
|
| [70] |
|
| [71] |
|
| [72] |
|
| [73] |
|
| [74] |
|
| [75] |
|
| [76] |
|
| [77] |
|
| [78] |
|
| [79] |
|
| [80] |
|
| [81] |
|
| [82] |
|
| [83] |
|
| [84] |
|
| [85] |
|
| [86] |
|
| [87] |
|
| [88] |
|
| [89] |
|
| [90] |
|
| [91] |
|
| [92] |
|
| [93] |
|
| [94] |
|
| [95] |
|
| [96] |
|
| [97] |
|
| [98] |
|
| [99] |
|
| [100] |
|
| [101] |
|
| [102] |
|
| [103] |
|
| [104] |
|
| [105] |
|
| [106] |
|
| [107] |
|
| [108] |
|
| [109] |
|
| [110] |
|
| [111] |
|
| [112] |
|
| [113] |
|
| [114] |
|
| [115] |
|
| [116] |
|
| [117] |
|
| [118] |
|
| [119] |
|
| [120] |
|
| [121] |
|
| [122] |
|
| [123] |
|
| [124] |
|
| [125] |
|
| [126] |
|
| [127] |
|
| [128] |
|
| [129] |
|
| [130] |
|
| [131] |
|
| [132] |
|
| [133] |
|
| [134] |
|
| [135] |
|
| [136] |
|
| [137] |
|
| [138] |
|
| [139] |
|
| [140] |
|
| [141] |
|
| [142] |
|
| [143] |
|
| [144] |
|
| [145] |
|
| [146] |
|
| [147] |
|
| [148] |
|
| [149] |
|
| [150] |
|
| [151] |
|


