作者简介:王水龙(1988-),男,浙江江山人,博士研究生, 主要从事实验地球化学研究. E-mail:shuilongwang0@126.com
岩浆演化过程中岩浆—流体阶段发生的相转变过程控制了元素在两相之间的分配行为。作为与岩浆热液活动有密切成因联系的金矿床,其在硅酸盐熔体和流体中的性状及两相间的分配行为是控制该类矿床成矿的重要物理化学因素。介绍了金在流体、熔体中的性状,论述了其在流体/硅酸盐熔体间的分配行为不仅受温度、压力、氧逸度等物理化学条件的影响,还受流体组分(阴离子、阳离子)、熔体组成(Na2O+K2O/Al2O3,Na/K,SiO2,NBO/T)的制约;最后对目前实验研究存在的问题、改进方法以及今后的研究方向进行了探讨。
Porphyry deposit is a kind of important ore deposit. Phase transition of Magma-Fluid stage in magma evolution controls the element distribution between different phases. Gold distribution between Melts and Coexisting Fluids is a important key to the metallogenic mechanism of porphyry deposits. The distribution of gold between different phases is not only controlled by temperature, pressure, oxygen fugacity, but also influenced by the content of fluids and composition of melts. Finally we reviewed the problems in experiment and future research on the partitioning of Au between melt and coexsiting fluids.
从全球范围来看,浅成热液型和斑岩型金铜矿床在时空上与侵入岩浆作用有关,岩浆和热液过程的共同作用形成了此类矿床[ 1]。斑岩型矿床是铜、金、钼的重要储库[ 2, 3],占据世界现在9%的金产量和57%的铜产量[ 4]。长英质岩石与浅成热液型和斑岩型矿床在时空上的联系吸引了大量学者,研究发现此类矿床是由出溶于岩浆储库的岩浆热液流体所含的金属元素沉淀形成[ 3]。元素在流体和熔体间交换、分配过程是岩浆热液矿床形成的重要环节[ 5]。因此,研究金在硅酸盐熔体和流体中的分配行为及其影响因素是认识中酸性岩浆演化与成矿机理的主要关键点。
约从20世纪40年代起元素的分配系数开始引入到结晶分异、蒸发岩、矿床形成的温度指示等地质研究中[ 6]。McIntire[ 7]首先对分配系数在地质学中应用的理论和实例作了系统的评述。1971年,Brett[ 8]根据球粒陨石或石铁陨石中分异的金属相和硅酸盐相中元素的丰度估算了金在金属相与硅酸盐相间的分配系数为130,这是文献中关于金在两相间分配最早的数据。
随着实验地球化学的发展,元素在流/熔体间的分配行为引起广泛关注。学者们相继开展了金的性质及分配行为的实验研究工作,这些实验以合成硅酸盐或天然岩石粉末作为熔体相,以水、氯化物、硫化物等作为气液相,来观察金在气相/液相、液相/熔体相、气相/熔体相之间的分配行为,或者是熔体相与一些常见硫化物矿物相之间的分配行为,取得了一些重要的数据[ 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34]。目前得到的数据指出金在流体/熔体间分配系数范围大致在几十到几百,硫化物固溶体/熔体间分配系数范围在几千到几万之间。前人研究大都侧重流体相成分变化对于金分配行为的影响[ 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34],而熔体组分对金分配行为的影响目前仅有少量涉及实验[ 32],金在气相和硅酸盐熔体相的性质及两相间分配行为也尚待进一步研究。
金在元素周期表中位于第6周期、ⅠB族。因在镧系元素之后,原子内部4 f14电子亚层全部充满,引起镧系收缩。随着核电荷数的不断增加,而原子内部半径增加不大,导致核电荷对外层电子吸引力增强,因而金的外层价电子不易失去。因此,金具有高电离势、高电负性及高氧化-还原电位的化学特性,不易形成离子,常以原子状态存在,金在自然界中呈自然元素或金属互化物产出[ 35]。
成矿元素在流体中主要以配合物的形式存在,配合物的种类和性质决定了元素在流体中的溶解、迁移和沉淀行为[ 36]。金在热液中可以形成Au-S、Au-Cl、Au-As、Au-Te等配合物[ 35],这些配合物的稳定性取决于金元素本身的性质及温度、压力、pH、氧逸度等因素的影响。了解金配合物的存在形式、性质对金在热液流体中的迁移、分布以及沉淀富集成矿有重要意义。
1.1.1 温度
温度升高导致溶剂水的介电常数大幅度降低,导致离子缔合程度增强,进而使配合物稳定性增加,更容易迁移成矿元素[ 37]。随着温度升高流体中金属阳离子主要以低价态电中性的配合物存在[ 37]。在温度为450~1027℃,由NNO缓冲剂控制的氧逸度条件下,Au-H2O体系中金的溶解度随温度升高而增加,当温度增高100℃,金在水中的溶解度大致呈数量级增长[ 38]。其他体系的实验结果也显示在一定条件下金的溶解度随着温度升高而增大[ 39, 40, 41, 42, 43],理论计算与实验数据基本一致,只是变化的幅度稍有不同。
1.1.2 压力
在温度为427~1027℃、压力为100~1000MPa的条件下,温度增高100℃,会使金在水中的溶解度提高大约1个数量级,可如果单靠压力来达到这个效果,则需要增加约1000MPa[ 39],表明温度对金溶解度的影响远比压力大。因此流/熔体实验中的压力影响相对于温度可以忽略不计。但是在考虑气相分配的情况下,压力是不能忽略的重要因素。
1.1.3 氧逸度和溶液pH值
在自然界金原子十分稳定,通常以自然金的形式存在。在溶液中金可以形成2种氧化态Au+和Au3+, Seward[ 42]经计算发现在热液成矿体系中Au+占主导地位,只有在高氧化态的情况Au3+才能稳定[ 43]。在不同体系中,氧逸度和溶液pH值对于金溶解度都有重要影响[ 43],任何一个条件的改变都能造成金溶解度的变化。如在温度为250℃,压力为50MPa的Au-S体系中, pH值在7左右,log f O2在-37~-35之间,金配合物具有最高溶解度100μg/g,当pH或氧逸度其中任何一个条件改变都会造成金溶解度的急剧降低[ 43]。
根据Pearson的硬软酸碱理论的标准[ 44],金被认为是软金属更倾向于和软的碱(如HS-, S2O32-, SbS2-等)形成配合物。Au-S和Au-Cl是金配合物在热液中的主要存在形式,目前已有相对多的数据,主要以实验研究及理论模拟方式展开。在天然水体系,HS-, S2O32-, SbS2-等配位体浓度很低的情况下, AuOH(H2O)0是最稳定的无机金配合物[ 45]。
Au-S配合物的物种形式相对复杂,目前的研究技术对于其物种形式又很难准确测定,目前Au-S配合物大都是基于数据的推理。一些学者对Au-S配合物进行了探索性的研究[ 46],认为酸性、近中性、碱性含硫热液中主要物种分别为Au(H2S)HS0或Au(HS)(H2O)0、Au(HS)2-、Au(SH)(OH)-1,在热液中对金的迁移有重要作用。另外,S2O32-也可能是重要的配位体[ 46],是金迁移的重要载体。
Au-Cl体系中配合物相对Au-S简单,主要形式为AuCl2-[ 46],只有在非常氧化的条件下,Au3+才能形成稳定的配合物。高温富氯热液流体中Au+-Cl为金的主要溶解迁移形式,AuCl2-相对于AuCl4-更为稳定[ 46]。
Tossell[ 47]运用从头算法Hartree-Fock MO对金在各种溶液中的配合物结构、能量、光谱进行了研究,指出各种条件下金的主要配合物形式。Liu[ 48]用第一性原理分子动力学模拟(first-principles molecular dynamics simulations)来研究在代表性地质条件下Au-S配合物。得到一些认识:①以前假设的Au(HS)(H2S)3 和Au(HS)物种在成矿条件下并不稳定;②低压条件下物种稳定性顺序Au(HS)2- > Au(HS)(H2S) > Au(HS)(H2O),高压条件下Au(HS)(H2S)会发生去离子化形成Au(HS)2-,只有Au(HS)2-和Au(HS)(H2O)稳定。③金离子溶解主要通过配体和周围水氢键的相互作用。
金在热液流体中主要以Au-S和Au-Cl配合物形式溶解迁移,配合物种类不同导致多种沉淀机制。温度、pH值、氧逸度、配合离子种类及浓度、沸腾、硫化物沉淀等因素改变都能引起金的沉淀。若金以Au-S配合物形式迁移,硫活度降低、溶液沸腾或稀释、氧逸度增加、pH值减少、温度降低都会引起Au的沉淀;以Au-Cl形式迁移时,氯化物活度降低、溶液沸腾、PH值增高、温度降低也会导致金沉淀出来[ 42]。在实际情况中可能更为复杂,在350℃以下,金的溶解和沉淀主要由反应⑴和⑵控制,但是温度大于350℃时AuCl2占支配地位,由反应⑶控制。根据勒夏特列原理,氧逸度和HS-, Cl-活度降低及PH值增大都能引起金的沉淀。但是在Au-S配位体系中温度降低并不一定会引起大规模的金沉淀,这一现象在Au-Cl体系表现的十分明显。举例来说,在300~500℃范围内,以50MPa下AuCl2-的稳定常数来计算,50℃的降温就能引起流体中95%的金沉淀,但对于Au-S配合物,温度降低金的溶解度却反而因为二硫化物稳定性增加而增大,进而重新活化进入浅成热液环境中[ 43, 49]。
Aus+ HS-+ H++ 1/4O2= Au(HS)0+ 1/2H2O ⑴
Aus+ 2HS-+ H++ 1/4O2= Au(HS)2-+ 1/2H2O ⑵
Aus+ 2Cl-+ H++ 1/4O2= AuCl2-+ 1/2H2O ⑶
某些难挥发金属元素也可以进入气相流体,如富气流体包裹体中Cu,Fe,Pb,Zn已达成矿浓度,现代火山喷气的凝结物中含有高浓度的Cu,Au,Zn,Pb,As,Ag,预示这些金属能以气相形式搬运[ 50, 51, 52, 53]。以前对于金属元素在气相中的行为了解很少,随着新技术的发展(PIXE,SXRF,LA-ICP-MS),对单个流体包裹体的成功测试分析,认识到气相在岩浆热液体系中对金属元素迁移的重要性,也是一种可能的成矿机制。岩浆热液金矿中,岩浆分异产生的气体也对金的迁移有部分贡献,一些斑岩和浅成低温热液金矿中的包裹体的气相中含有比共存盐水更高的金浓度也证明了这一点[ 54],表明当气相与液相共存时,气相拥有更高的分配系数,金更容易进入气相中。金在硅酸盐熔体、卤水、蒸汽中的分配实验证实了气相对于金的迁移能力[ 24, 25, 26, 54, 55, 56, 57, 58],在温度为800℃,压力为120MPa,ω(NaCl)为9%时,金在气相与熔体相间的分配系数达到56[ 25]。
阳离子在熔体中结构位置主要取决于离子强度,即离子电荷与离子半径平方之比 Z/R 2。Si4+作为中心阳离子构成Si-O4四面体网络结构,称为成网阳离子。其他高电荷小半径离子Al3+,Fe3+,Ti4+,P5+也能在熔体中呈四次配位而成为成网阳离子;K+,Na+,Ca2+,Mg2+主要以六次配位或更高次配位存在于四面体络阴离子之间的位置,改变熔体的基本结构和物理性质,称为变网阳离子[ 59]。
Connors[ 60]认为由于较高聚合度的高硅流纹岩不能容纳高含量的微量元素,包括金,这暗示金可能是通过Au-O配合形式溶解在硅酸盐熔体中。在没有S,Cl的体系中Au-O被认为是金在硅酸盐中的主要形式[ 1, 22, 32, 33, 34, 61, 62, 63, 64]。方程可以沿用Borisov[ 64]的表达:
Aumetal+ x/4 O2 = AuOx/2 ⑷
X为金在硅酸盐中的价态,AuOx/2为金溶解的形式,假定金的活度为常数,则得反应⑷的平衡常数:
log Au = x/4 log fO2+ C ⑸
C为与平衡常数和金摩尔分数有关的常数。根据log Au和log fO2为坐标投图,据此推测金的价态,认为AuO1/2是最主要的形式,这与实验数据基本上是吻合的[ 22, 64, 64]。
在温度范围为900~1250℃,压力为600~900MPa的条件下,金在硅酸盐熔体中溶解度随温度升高而增大,特别是在含Cl的情况下,金溶解度呈数量级增长[ 61]。Hoosain[ 64]的实验结果却发现压力对于金在熔体中的溶解度没有大的影响,跟流体中金溶解度受压力变化影响相似。在Au-O体系中,金溶解度随氧逸度升高而增大[ 22, 34, 64],但在含有硫、氯的硅酸盐体系中氧逸度跟金溶解度的关系就变得更为复杂[ 1, 22, 32, 33, 34, 64, 65, 66],特别在含硫体系中由于硫的多价态,氧逸度改变造成硫含量的变化进而影响Au-S配合物的种类和稳定性。
熔体中SiO2是决定熔体结构的最重要成分。在硅酸盐熔体中存在着桥氧(T)、非桥氧(NBO)和自由氧3种氧的结构状态,3种氧结构状态的比例和分布是决定熔体聚合程度的基本因素[ 67]。通常用每个硅氧四面体所含的非桥氧数量,即NBO/T比值,作为度量硅酸盐熔体聚合程度的参数[ 59]。随着SiO2含量的增高,熔体聚合程度逐渐增高,熔体中桥氧增多,自由氧和非桥氧迅速减少,NBO/T比值减小,熔体中能容纳的具有较高离子电位的阳离子越来越少[ 31]。化学组成不同的硅酸盐熔体的结构有明显的差异,熔体中金属阳离子(Na,K等)和挥发分F,C1含量的增加,使熔体中NBO/T的含量增大,熔体的聚合度减小[ 68]。目前相关的实验只有Zajacz[ 33]在温度范围在800~1030℃,压力在200MPa条件下对金溶解度与NBO/T比值和ASI(铝饱和指数)的关系进行了探索性研究,在含硫体系中随NBO/T值从0增加到0.5时金溶解度从0.25ng/g升高到3.25ng/g,而当ASI值0.7升高到1.15金溶解度从4.5 ng/g减小到0.25 ng/g。
硅酸盐熔体中F的加入能引起解聚作用,减低熔体粘度,增加阳离子和挥发分的扩散速率[ 68, 69, 70, 71, 72]。但是实验中硅酸盐熔体中F的加入并没有引起金溶解度明显的变化[ 61, 73],原因可能是F与金没有稳定配合物以及加入F的量还不足以显示出金溶解度。Cl的加入能引起金溶解度增大甚至呈数量级增加[ 3, 29, 61, 72, 74, 75]。金溶解度随S含量升高而增大[ 1, 3],金溶解度跟硫、氯活度还是呈现出良好的正相关关系[ 3]。
本文金的分配系数DAuL/M指在一定的温度、压力条件下,金在稳定共存的流体相(L)及熔体相(M)中的浓度比,此时金在两相中的化学势相等。根据能斯特分配定律,元素在熔流体间的分配系数受到温度、压力、体系成分的影响。大量的实验研究表明,成矿元素在流体和硅酸盐熔体间的分配行为除受温压、氧逸度等物理化学条件的制约外,流体、熔体组成及挥发分的含量也是影响金在两相间分配行为的相关因素。
流体成分阴离子配位体的种类和含量决定了所形成的配合物的种类[ 36]。不同流体成分的体系中,元素分配系数及其变化特征明显不同,这取决于流体介质中络阴离子与金属元素的结合能力。流体介质中阴离子活度的增加,有利于金进入流体相中。
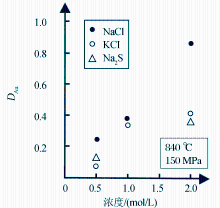
在温度为850℃,温度为150MPa条件下,纯水体系中,金的含量极低,以纯水为流体与花岗质熔体反应,金的浓度仅有0.09mg/L[ 29],对金的溶解搬运能力很弱。在含氯、硫体系中,流体中Cl-浓度或S2-浓度增加,金在流体/熔体间分配系数增大(图1)[ 11, 12, 24, 28, 29]。
花岗质硅酸盐熔体的结构是影响成矿元素分配行为的因素之一,在一定的温压条件下熔体结构主要取决于熔体成分,熔体NBO/T值对熔体中微量元素的分配行为有着明显的影响[ 5]。研究表明,在熔体NBO/T值升高的情况下Fe,Mn,Mg,K,Zn,Mo更倾向于分配进入熔体相中,导致元素的分配系数减小[ 76, 77, 78, 79]。
随着SiO2 含量和聚合程度的增加,元素的流体/熔体分配系数逐渐增大。干国梁[ 31]在文中提到Некрасов的实验数据显示,熔体组成从玄武质变为花岗质时,金在流/熔体相间的分配系数DAu 由4.5变为23.3,增大5倍, Zajacz[ 33]也指出SiO2 含量可能对金分配系数有影响。
Al3+在岩浆中既可以有四次配位而呈成网离子,也可能具有六次配位而作为变网离子,并且它取代四面体中的Si4+时需要碱金属和碱土金属离子的电荷补偿,因而使阳离子在岩浆结构中的位置复杂化[ 59]。随着K2O和Na2O含量的降低和Al2O3的含量的增高,进入六面体的Al3+越多。在1000℃、200MPa的条件下K2O/Na2O比值对于金的分配系数的影响并没有被观测到[ 32],而铝过饱和度的增加引起了金在气相与熔体相间分配系数的增大[ 33]。当熔体中含有硫、氯时,即使含量很低,也会对金分配有重要影响[ 32]。如图2所示,含硫体系中,在氧逸度低情况下具有较高的分配系数并随着熔体中硫含量的增加而升高,在氧逸度超过S2-/S6+转换界线之后,由于金与S6+ 形成配合物的物种及稳定性限制,金分配系数有很大幅度下降。
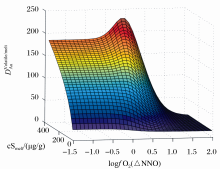 | 图2 金分配系数与氧逸度及硫含量关系[ 32]Fig.2 The relationship between gold partition coefficients and oxygen fugacity and sulfur concentration[ 32] |
目前,不同熔体组成对金在流体相与熔体相间分配行为的实验研究很少,没有足够的资料积累。流体的络阴离子Cl-浓度或S2-浓度增大和氧逸度升高[ 11, 12, 24, 28, 29],有利于金分配进入流体相。
从目前研究来看,关于金在熔体相/流体相/蒸汽气相间分配行为的实验研究是分散的,数据还很欠缺。以前的工作侧重于研究流体相成分对分配系数的影响,而对于熔体相组成对分配系数影响的研究却很少,但熔体结构也是影响元素分配行为的重要因素之一。在今后的研究中,应加强熔体组成变化对金分配行为影响以及金在三相间分配行为研究,探索不同熔体组分在斑岩型金铜矿床形成过程中的意义。
金配合物在高温高压下热力学性质还很有限,主要集中在 500℃以下,更高温或者超临界条件下的热力学参数还很匮乏。通过实验获得金配合物在超临界条件下的热力学参数,将是解释金的高温迁移和金成矿作用的重要理论基础。
现在常规的反应设备只能在反应后再取出样品进行测试,这样得到的数据与观测到的现象不可能实验条件时完全一样。因此,实现原位分析将是成矿模拟实验发展的重要方向。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|
| [61] |
|
| [62] |
|
| [63] |
|
| [64] |
|
| [65] |
|
| [66] |
|
| [67] |
|
| [68] |
|
| [69] |
|
| [70] |
|
| [71] |
|
| [72] |
|
| [73] |
|
| [74] |
|
| [75] |
|
| [76] |
|
| [77] |
|
| [78] |
|
| [79] |
|