张麋鸣(1989-),男,福建三明人,博士研究生,主要从事极地区域硫循环研究. E-mail: zhangmiming2010@163.com
二甲基硫(DMS)是一种重要的海洋生源硫化物, 通过海—气交换进入大气后生成生物源硫酸盐气溶胶从而对气候产生影响。海洋是大气DMS的主要源地, 海洋大气中约90%的DMS来自海洋。南大洋占世界大洋面积的20%, 是全球DMS重要的源之一。相较其他海域, 南大洋表层海水DMS存在显著的时空变化。由于南大洋复杂的水文环境、多变的海冰情况和受多种生物活动作用的影响, 完全了解这一区域DMS海—气交换过程及其控制因素变得更加复杂、困难。此外, 开展DMS的冰—气交换过程及其控制因素的研究也很有意义。为了便于今后在极区开展DMS海—气交换过程的研究, 深入探究极区DMS的生物地球化学过程。因此, 对南大洋DMS海—气通量的估算方法进行讨论, 分析南大洋表层海水DMS的分布特征及南大洋DMS海—气输送通量, 对南大洋DMS海—气交换过程的控制因素进行探讨。 [HT5H]
Dimethylsulphide (DMS) is an important marine biogenic gas and can be released into atmosphere through seaair gas exchange. The oxidants of DMS in atmosphere are the main compounds of pristine marine sulphate aerosols and would affect the global climate change finally. Almost all the atmospheric DMS, about 90%, comes from the ocean. The southern ocean, which consists about 20% of the whole ocean area, is one of the largest atmospheric DMS sources. In contrast with the other oceans, the Southern Ocean appears great spatial and temporal variability of surface seawater DMS. In addition, there are the complex hydrography system, variable sea ice condition and various biologic activities in the Southern Ocean as to make survey and understand DMS as well as its controlling factors most difficult. Moreover, it is significant to integrate the DMS seaice exchange processes and its controlling factors studies. In order to develop survey and research on the seaair DMS exchange and biogeochemistry processes, estimate methods of the seaair DMS fluxes will be reviewed, characteristics of the spatial and temporal distribution of surface seawater DMS will be discussed and the seaair DMS flux in the Southern Ocean will be assessed. Finally, major controlling factors of DMS seaair DMS processes will also be analyzed.
二甲基硫(Dimethylsulphide, DMS)是一种重要的海洋生源气体, 是参与全球硫循环的一个重要的组成部分, 在海洋与大气相互作用中扮演重要的角色。DMS由其前体二甲基巯基丙酸(Dimethylsulfoniopropionate, DMSP)通过藻类的酶或微生物酶解而来。DMSP由藻类利用海水中的硫酸盐经过一系列的反应合成产生, 不同藻类产生DMSP的能力有所不同。DMS通过海气交换进入大气后, 主要被大气中的自由基OH·, NO3·氧化, 产生甲磺酸(Methane Sulphonic Acid, MSA)、SO2等产物, SO2可以进一步参与形成非海盐性硫酸盐 (nss-SO42-), 成为海洋大气气溶胶的重要组成[ 1]。DMS氧化产物可参与形成云凝结核(Cloud Condensation Nuclei, CCN), 并增加CCN的浓度, 即通过生成新的颗粒物或使原有细小颗粒物长大至CCN粒径(> 约 50 nm)。CCN的增加提高了云层对太阳辐射的反射和散射率, 影响地表太阳辐射收支, 从而影响着全球的气候[ 2]。DMS是上层海洋与低层大气研究
(Surface Ocean and Lower Atmosphere study, SOLAS)的核心内容之一, 近几十年的研究表明, DMS在生物学、海洋化学、大气化学、环境化学、气候学等领域都有重要的研究意义。
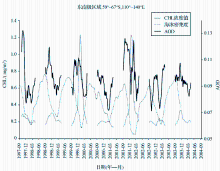
最新的研究表明, 全球海洋DMS的通量大约为28.1 Tg(S)/a[ 3], 不同学者给出的通量结果略有偏差。北冰洋、南大洋特别是南极海冰区, 被认为是大气DMS巨大的源, 并且对全球硫的收支有着重要的贡献。已有的估算表明, 仅仅是占世界海洋面积6%的南大洋南极区域(Antarctic Zone)和季节性海冰区(Seasonal Ice Zone), 占全球DMS总通量的17 %[ 4]。Kloster等[ 5]模拟全球不同季节全球海洋表层海水DMS平均浓度值的结果表明, 南大洋的春夏季具有较高的DMS浓度值, 说明南大洋向大气输送的DMS基本上来自于这2个季节。已有科学家发现, 南极进入春夏季后, 海冰面积大面积消退, 生物活动增强, 在季节性海冰区观测到表层海水叶绿素浓度与气溶胶光学厚度(Aerosol Optical Depth, AOD)存在一定的联系(图1)。并认为海冰融化所导致的生物量增加, 可产生大量硫酸盐气溶胶前体物质(主要为DMS), 这些物质进入大气后形成硫酸盐气溶胶, 并在一定程度上影响南极的气候[ 6, 7]。另外, Vallina等[ 8]的研究也证实了南大洋大气中CCN主要受到生源DMS释放的控制, 估算夏季生物来源贡献的CCN占80 %, 冬季约为35 %。由此可以说明, 南大洋生源DMS可通过海气输送进入大气并影响大气气溶胶的组成, 进而影响南极区域的气候。
南半球的高纬度地区(南极和南大洋)在全球气候系统中扮演着重要的角色, 在过去的气候变化以及当前和未来由人类活动引起的气候变化中起关键作用[ 9]。陈立奇等指出, 南北极变化对全球气候变化起到一种指示和调控作用, 南极地区可能会在2050年前后因臭氧空洞恢复而快速升温, 并引发东南极冰盖的融化及海冰覆盖面积的减少[ 10]。这就表明未来南极变化, 可能对南大洋DMS的生物地球化学过程产生一定的影响, 进而影响南大洋DMS的海—气输送通量。有模拟研究表明, 大气CO2的持续增加, 导致全球变暖趋势可能会增加南大洋DMS通量[ 11]。而DMS的通量增加所产生的负反馈作用, 是否会缓解南极区域的暖化过程还不得而知。因此, 在南大洋区域开展关于DMS及其相关物质的生物地球化学过程的研究就显得非常迫切且富有意义。
目前, 国内在南大洋区域硫循环的研究, 主要涉及到DMS相关的气溶胶观测[ 12], 而在海水及海冰领域DMS的观测仍处起步阶段。本文就南大洋DMS海—气交换过程这一方面进行讨论, 分析南大洋DMS海—气交换过程的控制及影响因素。
DMS海—气通量的估算对认识全球硫循环有重要的作用, 准确估算DMS海—气通量一直以来都是科学家们所致力于解决的难题。目前, DMS海—气通量估算方法, 主要有利用模型计算及直接测量2种方法。直接测量方法主要以涡旋相关法(Eddy Correction, EC)为代表, 即通过利用大气压离子质谱(Atmospheric Pressure Chemical Ionization Mass Spectrometry, APCI-MS)快速测定大气中的DMS, 得到空间上某一点的实时通量, 根据泰勒(Taylor)冻结湍流假说算得垂向的平均通量[ 13]。但是, APCI-MS由于价格昂贵, 且无商品化仪器, 仪器维护成难度较大, 并没有被广泛使用。当前运用得最为广泛的DMS海—气通量估算方法以模型计算为主, 以利用滞膜模型(Stagnant Film Model)为代表, 通常由下式得出[ 14]:
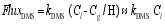 | (1) |
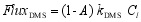 | (2) |
式中: kDMS为传输速率, Cl为DMS在表层海水中的浓度(nmol/L), Cg为DMS在大气中的浓度(nmol/m3), H为亨利常数。因为表层海水中的DMS浓度往往比大气中的DMS浓度高出约3个数量级, 所以公式(1)中 Cg/H项可以忽略不计。在南大洋季节性海冰区, 需要考虑海冰面积的影响, A为海冰覆盖率, 因此采用公式(2)计算该区域DMS通量值。要计算DMS的海—气通量值, 需要知道表层海水的浓度值 Cl和传输速率 kDMS, kDMS一般通过下式算得:
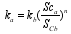 | (3) |
代入得:
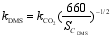 | (4) |
式中: kCO2为CO2的传输速率(cm/h), Sc为斯密特(Schmit)数( 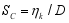
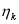
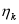
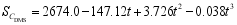 | (5) |
式中: t为海水的温度, 单位为℃。
表1列出了通过 kCO2 换算而来的用于计算DMS传输速率较为常用的经验表达式。其中, LM86的方法是在一个湖泊中, 利用SF6逸出速率和响应的风速推算的[ 17]。然而, 湖泊与海洋所处的环境有很大的不同, 所以LM86方法或许不太适用。N2000及W92的方法也是在近岸区域推算的, 运用于开阔大洋也有一定的误差。尤其在南大洋区域, 往往具有较高的风速, 而一般的方法在较高的风速条件下, 传输速率值的估算并不准确, 从而影响了高风速海区DMS海—气通量估算的准确性。但是, LM86, W92方法在海气交换通量计算中被运用得非常广泛。Ho等[ 18]利用3He/SF6双示踪技术, 在南大洋区域进行现场试验, 实验海域同时包括近岸和大洋区域, 并得出更适用于较高风速下(> 15 m/s)海—气传输速率计算值, 该法几乎可在全球海洋DMS海—气通量估算中使用。
| 表1 常用DMS传输速率表达式 Table 1 The expression of DMS transfer velocity |
此外, 表层海水DMS浓度值 Cl通常通过现场观测获得。目前用于观测海水DMS方法, 主要有吹扫捕集法、膜进样质谱法(Membrane Inlet Mass Spectrometry, MIMS)和大气压离子质谱法(APCI-MS)。最为常用的方法为吹扫捕集法, 由于其具有灵敏度高、检测限低(< 0.05 nmol/L)及需要样品量少等特点, 该法被迅速的推广, 许多科研工作者在此基础上对该技术做了改进并长期用于船载测定, 这不仅缩短了DMS的分析时间, 同时使所得的数据更加准确[ 21]。然而, 吹扫捕集法测定一个样品的时间仍较长, 一般 > 10 min, 限制了采样密度, 且吹扫捕集法自动化程度较低, 制冷多用不易保存的干冰及液氮, 无法实现长期连续测定。MIMS方法的出现, 使得高密度连续观测海水表层DMS浓度成为可能, 测样时间也大大缩短, 约20 s可采集一个数据, 并且可以实现自动观测[ 22]。然而, MIMS法的检测限为nmol/L级, 且由于表层海水在走航泵系统中存在DMSP酶解等生物活动, MIMS走航测量所得的DMS浓度值比用吹扫捕集方法测定Niskin 采水瓶采集水样的DMS浓度值高20 %[ 23], 表明MIMS方法仍存在一定的误差。另外, 还有一种方法是利用膜平衡进样的方式, 采用APCI-MS对海水及大气DMS进行连续观测, 仪器自动化高, 测样速度较快, 通常用于涡旋相关法(Eddy Correction, EC)直接测定DMS海—气通量[ 13]。
一般而言, 现场获得的DMS数据量偏少, 导致估算海区的DMS海—气通量具有很大的不准确性。遥感技术的出现, 为实现全面的、长时间系列的海表DMS观测提供可能。这样一来, 可以通过遥感技术对全球DMS海气通量进行估算。遥感技术并不是直接测量海水表层的DMS浓度, 而是通过测量叶绿素(CHL)浓度等参数, 通过叶绿素与海水表层DMS浓度经验关系估算而来, 下式为采用该方法的一个例子[ 24]:
CDMS= -Ln(MLD)+5.7 for CHL/MLD<0.02
CDMS=55.8Ln(MLD)+0.6 for CHL/MLD≥0.02 (6)
式中, CHL为叶绿素浓度, MLD(Mixed Layer Depth)为混合层深度, ln为自然对数函数。由此可以估算出表层海水DMS的浓度值, 并结合遥感观测的海表温度(Surface Seawater Temperature, SST)和风速, 利用估算DMS 海—气通量的经验公式进行大范围的模拟全球海域DMS通量的时空分布。遥感技术的估算仍具有一定的误差, 所以在估算全球DMS海—气通量时, 往往通过现场观测数据域卫星遥感数据相结合, 进行的估算值较为准确。
南大洋由4个最重要的亚系统组成, 由北向南分别是:极峰区(Polar Front, PF), 永久开阔大洋区(Permanently Open Ocean Zone, POOZ), 季节性海冰区(Seasonal Ice Zone, SIZ), 沿岸陆架区。因而在南大洋区域, 可以发现明显的温度、盐度、叶绿素、营养盐等经向方向上的变化, 导致南大洋生产力在不同区域上有所差异。南大洋是典型的高营养盐低生产力(High Nitrient Low Chlorophyll, HNLC)海域, 其大部分的区域生产力很低, 并且在开阔海域的生产力变化很小。然而在近岸/陆架区, 季节性海冰消退区/陆缘冰带, 以及南极峰毗邻地带容易发生浮游植物的水华, 并具有较高的生产力[ 25]。由于DMS是由浮游植物产生的DMSP转化而来, 一般来说DMS和叶绿素有明显的正相关关系, 所以在南大洋表层海水的DMS分布与叶绿素及生产力的分布情况大有很大的关系。此外, 南大洋表层海水DMS浓度高值出现在春夏季, 而秋冬季节由于海冰的覆盖DMS浓度值很低。
如图2, 为Tortell 等[ 26]首次利用MIMS方法对南大洋海域进行观测, 航迹从新西兰到罗斯海(Ross Sea)冰间湖区域, 得到了11 ~ 12月期间DMS, pCO2, △O2/Ar等高分辨率的表层海水走航数据。该研究证实, 在南极季节性海冰区小尺度的范围内 (< 10 km), DMS表层海水的时空变化很大, 且开阔海域与季节性海冰区有显著地不同。由图2可得, 南极极峰区及无冰的永久开阔大洋区的DMS浓度值不会很大(< 5 nmol/L), 在极峰处可以观测到较高的叶绿素值, 并与之对应稍高的DMS浓度值。这是因为南极极峰区及永久开阔大洋区总体上生产力不高, 而导致DMS浓度值不高。在南大洋印度洋扇区[ 27], 太平洋扇区[ 28]及大西洋扇区[ 29]的海水表层DMS观测结果也表明, 在南极极峰区及永久开阔大洋区的DMS浓度值基本都< 5 nmol/L, 由此可以说明南大洋大部分的海域DMS浓度值不高。这一区域与东北太平洋HNLC海域表层海水DMS的浓度数值范围较为一致[ 30]。Lana等[ 3]对全球表层海水DMS浓度模拟值表明, 南大洋极峰区及永久开阔大洋区春夏季表层海水DMS浓度值基本都< 5 nmol/L, 但南大洋区域表层海水DMS浓度值明显高于其他海域。从图2还可以发现, 由永久开阔大洋区进入季节性海冰区时, 海冰边缘区域往往有较高的DMS浓度值, 有研究观测结果表明这一数值甚至可以达到几十个nmol/L[ 27]。表层海水DMS 在季节性海冰区中的分布情况与海冰覆盖率有很大的关系, 当海冰覆盖率较低时(约小于80 %), 表层海水DMS浓度较高。然而, 当海冰覆盖率很高时DMS浓度值反而较低(图2), 有研究发现, 海冰覆盖率 > 80 %区域DMS浓度值甚至< 1 nmol/L[ 31]。在近岸陆架区冰间湖区域, 表层海水浓度值, 总体上比较高, 且DMS浓度值分布变化较大, 并具有一定的季节性变化。早春时期, 由于太阳辐射的加强和融冰过程的影响, 冰间湖区域容易发生水华, 此时DMS浓度比较高。在罗斯海冰间湖的观测表明, 春季冰间湖区域的表层海水DMS平均浓度(19 nmol/L)较夏季DMS平均浓度(8.7 nmol/L)高2倍[ 32]。在阿蒙森海(Amundsen Sea)季节性海冰区及冰间湖区域的观测结果显示, 表层海水DMS的浓度变化范围可由低于1 nmol/L至350 nmol/L, 且在冰间湖中部海域DMS浓度值基本 > 100 nmol/L, 这种变化与海域水文条件及浮游生物量变化有关, 并证实了在陆架区北部的开阔大洋区域、浮冰区及冰间湖区, DMS分布情况有显著的不同[ 23]。综上所述, 南大洋表层海水DMS分布与其他区域有明显的不同, 南大洋极峰区和永久开阔大洋区的DMS浓度值一般较低。在南大洋季节性海冰区, 表层海水DMS浓度值受海冰覆盖率的影响, 波动较大。而在近岸陆架区冰间湖区域, 往往表现出较高的DMS浓度值, 这与区域水文条件及浮游植物量的变化相关。
南大洋DMS海—气交换通量与表层海水DMS分布较为一致, 在极峰以南的季节性海冰区及陆架区, 往往具有较高的通量值。Curran等[ 33]首次整理了由澳大利亚至南大洋7个航次(1991~1995)的DMS数据, 并估算出DMS在夏季亚南极区域(Subantarctic Zone, SAZ;包括极峰区及永久开阔大洋区)、南极区域(Antarctic Zone)及季节性海冰区域的通量, 分别为6.7, 20和49 µmol/(m2·d), 春季亚南极区域及南极区域分别为3.8和1.7 µmol/(m2·d), 春夏季平均通量为9.4 µmol/(m2·d), 并指出海冰的DMS交换通量并未纳入计算, 导致均值的估算偏低, 认为海冰区是大气DMS一个重要的源。然而, 不同学者估算的冰—气DMS通量有很大的不同。Nomura等[ 34]首次利用箱式技术直接测定了南极浮冰(Pack ice)的DMS通量, 估算有雪层覆盖时DMS通量为0.1 ~ 0.3 µmol/(m2·d), 无雪层覆盖时DMS通量为0.1 ~ 5.3 µmol/(m2·d)。而Trevena 等[ 35]在季节性海冰区估算的DMS通量较大, 11 ~ 12月季节性海冰区 海冰DMS平均通量为25 µmol/(m2·d), 浮冰的通量最高54 µmol/(m2·d) (1 ~ 325 µmol/(m2·d)), 其次是固定冰(Fast ice)16 µmol/(m2·d) (10 ~ 50 µmol/(m2·d))、边缘冰(Ice edge)12 µmol/(m2·d) (1.2 ~ 26 µmol/(m2·d))。造成这种估算偏差的原因在于, 海冰中DMS浓度测量方法有较大误差, 通量的估算方法也不相同。另外, 在季节性海冰区冰间湖区域, 有较大的DMS通量值。在罗斯海区春夏季估算的DMS平均通量分别为(40 ± 30), (20 ± 20) µmol/(m2·d)[ 32], 阿蒙森海冰间湖区估算通量平均值为23.1 µmol/(m2·d)[ 23]。总体来说, 在南极区域和季节性海冰区的DMS通量与海水表层DMS浓度分布相关, 在季节性海冰区的通量值变化较大, 其中冰间湖区域有较大的DMS通量, 并且都具有明显的季节变化性, 春夏具有较高的通量值。
由第2节可知, DMS海—气通量估算涉及海表DMS浓度值及 kDMS。 kDMS可以通过海水的温度、盐度及风速算得。海水中DMS 由浮游植物产生的DMSP酶解而来, 通过海气交换、微生物降解及光降解去除。控制DMS表层浓度的因素主要有:浮游植物种类、海气交换过程、微生物降解、光降解过程等[ 36]。在南大洋区域, 海冰的变化对全年DMS海—气输送通量有巨大的影响, 海冰覆盖面积的变化直接影响了DMS海—气交换面积的大小, 这一变化是南北极海域特有的。此外, 南大洋区域复杂的水文环境也会有一定的影响, 如近岸区域绕极深层水(Circumpolar Deep Water; CDW)的涌升, 改变表层海水的温盐特性, 并影响包括DMS在内的与生物相关溶解气体的分布;融冰过程可以加剧海水的层化, 有益于DMS在表层海水中聚集等[ 23], 同时海冰的融化也对周围水体贡献了一定的DMS及营养物质, 这也对DMS的分布产生影响。综上所述, 南大洋区域DMS海—气交换过程受生物因素及非生物因素2个方面共同作用, 大部分海域生物因素控制更为显著。生物因素主要包括浮游植物的组成及微生物的降解。非生物因素主要包括海冰融化影响、水文环境、DMS光降解过程等。
 | 图2 南大洋区域2个断面的表层海水观测数据(2006.11 ~ 2006.12)(a)SeaWiFS 8天平均叶绿素数据, 红线(向北航行)和黑线(向南航行)分别代表船的航线, 白色区域代表海冰或云层覆盖区域;(b)船载走航荧光观测叶绿素数据;(c)走航表层海水温度(SST)及海冰覆盖率。箭头表示北亚南极峰(NSAF), 南亚南极峰(SSAF), 极峰(PF), 南极绕极流南部峰(SACCF)位置;(d)走航表层海水△O2/Ar及净生产力(NCP, Net community production)数据;(e)走航表层海水pCO2值, 虚线为大气pCO2值(f)走航表层海水DMS浓度值[ 26]Fig 2 Surface water property distributions along two Southern Ocean transects, Nov ~ Dec. 2006.(a)Chlorophyll α concentrations were derived from Sea WiFS 8-day men composite data , red line (Northward)and black line(Southward) show the ship position, while white areas denote the presence of sea ice or cloud cover;(b)ship-based underway fluorometric analysis Chlorophyll αconcentration;(c)Surface seawater temperature and ice cover rate;(d)Surface seawater △O2/Ar value and NCP value.(e)Surface seawater pCO2 data and Dashed line shows the atmospheric pCO2 level;(f)Surface seawater DMS concentrations[ 26] |
4.1.1 浮游植物影响
浮游植物对南大洋区域DMS产生有重要的影响, 进而影响DMS海—气交换过程。产生DMSP的主要浮游植物有球石藻( Coccolithophores)、棕囊藻( Phaeocystics)、甲藻( Dinoflagellates)等, 硅藻( Diatoms)只能产生较少的DMSP[ 1]。南大洋极峰区域的优势藻种为硅藻, 在近岸冰间湖区域, 例如罗
斯海冰间湖, 优势藻种可为棕囊藻和硅藻, 且优势藻种变化与季节相关[ 32]。南大洋极峰区存在铁限制, 生产力不高, 并且优势藻种为产生DMSP偏低的硅藻, 可供酶解的DMSP量并不多, 进而影响DMS的产生, 并使这一区域DMS海—气输送通量值不高。虽然有研究指出, 在铁限制的情况下, 可刺激藻细胞产生更多的DMSP[ 37], 但是极峰区生物量偏低是影响表层海水DMS浓度值低的重要原因。此外, 极峰以北的区域还存在硅限制, 这也会影响硅藻的生长。而极峰以南, 在CDW上升流的影响下, 从深海带来丰富的硅酸盐物质[ 25]。在季节性海冰区, 特别是冰间湖区域, 海冰融化及陆源物质输入使得这一区域不在受到铁的限制, 具有较高的生产力[ 23], 这是造成这一区域表层海水DMS浓度高值的主要原因。在罗斯海冰间湖的研究表明, 早春时期冰间湖区域容易发生棕囊藻水华, 是表层海水具有较高的DMS浓度值主要原因[ 32]。然而在南极的夏季, 虽然海冰区冰间湖区域也同样具有很高的生产力, 但是控制表层海水DMS浓度可能不仅仅是浮游植物的作用, 还可能与微生物降解及水文条件的变化有关。
4.1.2 微生物的降解影响
微生物对DMS的降解过程, 被认为是海水中DMS迁出的主要途径, 在北海区域的研究表明, 微生物降解迁出DMS的比重占50 % ~ 80 %[ 38]。微生物降解速率(Biological Consumption Rate, BDMSC)的大小, 取决于海域微生物的种类及海水的温度。在南大洋区域, 海水的温度较低, 微生物的降解作用不强。因为在南大洋区域DMS微生物降解的研究非常少, 主要集中于罗斯海区域, 所以很难描述整个南大洋区域微生物DMS的降解情况。较其他海域, 南大洋区域微生物降解速率变化较大, 微生物降解速率值较低, 且春夏季节有所差异, 夏季由于海水温度较高表现出较高的微生物降解速率值(表2)。春季较低的微生物降解速率值, 又容易发生浮游植物的藻华, 使DMS在表层海水中聚集, 从而表现出较高的DMS浓度值[ 39]。夏季较高的微生物降解速率值, 也被认为可能是罗斯海冰间湖区域夏季表层海水DMS平均浓度值较春季该区域DMS均值低2倍的主要原因[ 32]。微生物降解速率值表现出的时空变化, 会影响DMS的海—气交换过程。
4.2.1海冰的影响:
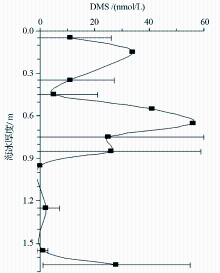
海冰中含有冰藻, 大部分为硅藻, 使海冰含有一定DMSP, 由此可产生DMS[ 43], 在浮冰、固定冰及边缘海冰中均可发现含有DMS, DMSP[ 35]。海冰中存在许多细微的通道, 这些通道控制了海冰中气体的释放量, 通道的大部分都填满了卤水(brine), 海冰中DMSP转化成DMS的过程及其向大气释放DMS的过程都会通过海冰中的通道网[ 44]。图3为典型的海冰中DMS垂向分布图[ 35]。一般而言, 海冰的通道水中含有较高的DMS, DMSP浓度值, 尤其是在海冰的底部, DMS, DMSP的浓度较海冰底部水体中的DMS, DMSP浓度值高很多, 这种差值甚至可达20 ~ 500倍不等[ 28]。Tison等在威德尔海西部冰架区域发现, 底部的冰中含有极高浓度的DMS, DMSP, 分别为636 ~ 2637 nmol/L, 292 ~ 1430 nmol/L[ 45]。在在吕措—霍尔姆湾(Lützow—Holm Bay)采集的冰柱样中DMS, DMSP分析研究表明, 海冰底部DMSP+DMS的浓度可高达110 nmol/L, 并具有较高的叶绿素浓度(高达239.3 μg/L), DMSP+DMS浓度与叶绿素浓度具有很好的正相关关系, 此外通过计算得出海冰通道中盐水的DMS+DMSP平均值可高达332.4 nmol/L[ 46]。这说明, 海冰中也具有很高的生产力, 并因此而具有较高的DMS, DMSP浓度值, 且不同区域冰样中DMS, DMSP浓度也有所差异。当海冰发生融化时, 海冰中的DMS, DMSP及冰藻一并进入周围的海水中, 使周围的水体及冰下水体具有高的DMS值。海冰如同DMS点源(hot spot), 向周围的水体输送高浓度的DMS, DMSP[ 43], 这也可以用来解释在季节性海冰区及冰间湖区表层海水DMS浓度值在小尺度范围内变化较大的现象[ 26]。海冰融化输送的冰藻等浮游植物可以作为周围海水中初始的浮游植物进行生长, 一些微量营养元素(如铁)也会进入海水中, 并有益于浮游植物的生长[ 44]。此外, 海冰融化使周围表层海水的盐度降低, 加剧海水的层化, 有利于DMS在表层海水的聚集, 从而影响表层海水DMS的浓度值, 并最终影响DMS海—气交换过程。海冰融化的影响在早春时期较大, 此时大面积的海冰融化与浮游植物的爆发存在一定的联系。然而在阿蒙森海夏季观测表明, 只有1 %的数据在叶绿素浓度值< 1 μg/L 时表层海水DMS的浓度值 > 20 nmol/L, 说明夏季海冰融化可能对DMS的影响较小[ 23]。在全年尺度上海冰面积的消涨, 不仅对南大洋整个生态环境的影响重大, 同时对DMS海—气交换过程有很大影响, 尤其是在季节性海冰区和沿岸陆架区由冬季到夏季DMS海—气交换通量的巨大差异变化。
4.2.2水文环境及光降解的影响
在南大洋极峰区域, 极峰所处的位置, 可能由于生产力高些而改变浮游植物生物量, 进而影响表层海水DMS浓度值, 这一区域水文环境较为简单, 不是影响表层海水DMS浓度值的主要因素。极峰区由于存在常年西风带, 往往具有较高的风速, 甚至 > 15 m/s, 高的风速使这一区域具有较高的海气交换速率[ 18]。靠近陆架区及季节性海冰区, 水文环境更为复杂, 表层海水DMS浓度值受水文因素影响, 主要包括混合成深度变化、部分区域变性南极绕极流(MCDW)的涌升、海冰融化等。以Tortell等[ 23]在阿蒙森海的研究为例, 在夏季Pine Island 冰间湖区(PIP)中部开阔水域, 由于较高的海表温度, 层化作用强烈, 混合成深度变小, 生物活动显著, 表现出较高的生产力, 表层海水DMS容易聚集并具有较高的浓度值(可达上百nmol/L)。而靠近PIP南部Pine Island Glacier(PIG)的近岸区域, 水文环境有明显不同。由于PIG南部存在MCDW的涌升, 涌升区域生产力并不高, 然而在PIG东北部却有极高的叶绿素值。可是表层海水DMS在PIG的浓度值并未与PIG南部及东北部的叶绿素值相对应, DMS的浓度高值出现在MCDW涌升区域偏北的位置, 分析可能与PIG湾内顺时针的环流及微生物的降解限制有关。在PIG的北部的浮冰区域, 海冰融化的影响没有早春时期明显, 说明夏季海冰融化对表层海水DMS浓度值的影响较小[ 23]。而在罗斯海, 由于宽广的陆架限制了MCDW涌升至近岸区域, 冰间湖表层海水温盐特性受海冰及太阳辐射影响较大, 由此导致的混合成深度的变化会在一定程度上影响表层海水DMS浓度[ 32]。此外, 在威德尔海(Weddell sea)冰架区发现在多年冰中含有极高DMS浓度值[ 47], 由冰架产生的冰架水或多或少也会对冰架边缘海水DMS浓度值造成一定的影响。总的来说, 水文环境变化对表层海水DMS浓度分布可产生很大的影响, 是影响表层海水DMS分布的一个重要控制因素。
相对于其他因素, DMS光降解的研究相对较少。通常情况下, DMS主要在可见光区被降解, 与有色溶解有机物质(CDOM)有关, 在380 ~ 460 nm波段降解速率最大, 光降解在海水的DMS迁出中占的比重不大[ 1]。在南大洋区域, DMS光降解的研究非常少。有研究指出, 在南大洋营养盐较高的区域, 早春时期在未发生藻华及无海冰覆盖区域DMS光降解的速率较高, 为海水DMS主要迁出途径[ 41]。这可能是因为, 早春时期海冰刚刚融化, 海水温度低, 微生物的降解受到抑制, 导致光降解为主要的迁出途径。
目前, 虽然在南大洋DMS的观测数据已经占全球观测数据的1/5(引自http://saga. pmel.noaa.gov/dms/), 但是由于表层海水DMS在一些区域, 特别是在季节海冰区存在明显的时空变化, 表层海水DMS浓度值在小尺度范围内可从无法检出变化至上百nmol/L, 使在南大洋海域准确估算DMS海—气输送通量变得极为困难、复杂。加之人类对海冰DMS的研究才刚刚开始, 更加无法准确估算海冰对大气DMS的贡献。此外, 在模拟全球DMS通量时, 有的研究将海冰覆盖率 > 75 %的区域假设为没有DMS通量输出[ 3], 然而事实上这些区域是具有一定DMS通量的, 在这种情况下会低估总的DMS通量值。所以, 一方面要改进和发展高效、灵敏的海水及海冰DMS观测方法, 并运用到实际的现场观测中, 以便获取大量的数据。另一方面, 针对极地区域, 需要更加细化及完善DMS通量估算模拟方法, 以便获得更准确的估算值。
另外, 在南大洋DMS相关研究主要集中于无海冰覆盖的极峰区域及罗斯海、阿蒙森等少数冰间湖海域, 还需要进一步扩大DMS研究范围, 积累海冰区、陆架冰区海冰及海水DMS时间空间分布数据, 深化在南大洋区域DMS生物地球化学过程的研究, 便于准确估算南大洋DMS通量, 并最终为了解南大洋大气层气溶胶的组成变化及其所带来的气候影响提供有力的数据支持。而未来, 在全球气候变暖背景下, 南大洋海冰可能会发生的变化对该区域DMS生物地球化学过程会带来什么样的影响, 以及这些改变是否会发生如CLAW假说那样的负反馈作用还无法预知。同样, 海洋酸化对极区生态系统可能造成的影响, 是否会对DMS的产生及通量变化带来影响也无法知晓。所以, 开展南大洋DMS的海—气交换过程的研究, 进一步深入探究DMS在极地区域的生物地球化学过程, 是非常有必要也富有意义的。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|